Ósmio - Os
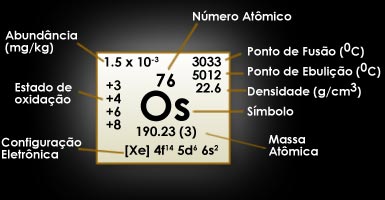
Forma química na solução: OsCl62-
Cor da solução aquosa: Esverdeada
Compatibilidade Química: Somente deve ser diluído com HCl 5%. Pode ser diluído com outros metais e ânions somente em HCl 5%. Não diluir com HNO3 pois pode formar OsO4 muito volátil e tóxico.Outros ânions oxidantes como peróxidos, Cr2O7--, ClO-, ClO2- e ClO3- se presentes também podem formar OsO4.
Estabilidade: A solução é estável por anos em frascos de polietileno (LDPE) em concentrações de 1 - 10.000 mg/L em HCl 10%. Em concentrações de 0,001 - 1 mg/L não é conhecida a sua estabilidade.
Preparação de Amostras:Deve-se tomar muito cuidado em preparações de amostras principalmente porque o Os é facilmente oxidado a OsO4 volátil e provocando perda do metal. O metal é atacado pela água régia formando OsO4 volátil. O metal pode ser atacado também pela passagem de Cl2 em uma mistura de pó de Os com KCl. Forma-se o K2OsCl6 que pode ser extraído com água. A fusão de seus minerais e ligas com KOH/KNO3 pode ser usada já que forma Osmato de Potássio (K2OsO4) que é solúvel em água e HCl. Não digerir com HNO3 e nem diluir com este ácido.
Manuseio e armazenagem: Manter o frasco fechado quando não estiver usando. Armazenar a 20oC +/- 5oC. Evitar retorno de solução para o frasco. Não pipetar diretamente do frasco para evitar contaminações.
Informações espectrais:
Cor da solução aquosa: Esverdeada
Compatibilidade Química: Somente deve ser diluído com HCl 5%. Pode ser diluído com outros metais e ânions somente em HCl 5%. Não diluir com HNO3 pois pode formar OsO4 muito volátil e tóxico.Outros ânions oxidantes como peróxidos, Cr2O7--, ClO-, ClO2- e ClO3- se presentes também podem formar OsO4.
Estabilidade: A solução é estável por anos em frascos de polietileno (LDPE) em concentrações de 1 - 10.000 mg/L em HCl 10%. Em concentrações de 0,001 - 1 mg/L não é conhecida a sua estabilidade.
Preparação de Amostras:Deve-se tomar muito cuidado em preparações de amostras principalmente porque o Os é facilmente oxidado a OsO4 volátil e provocando perda do metal. O metal é atacado pela água régia formando OsO4 volátil. O metal pode ser atacado também pela passagem de Cl2 em uma mistura de pó de Os com KCl. Forma-se o K2OsCl6 que pode ser extraído com água. A fusão de seus minerais e ligas com KOH/KNO3 pode ser usada já que forma Osmato de Potássio (K2OsO4) que é solúvel em água e HCl. Não digerir com HNO3 e nem diluir com este ácido.
Manuseio e armazenagem: Manter o frasco fechado quando não estiver usando. Armazenar a 20oC +/- 5oC. Evitar retorno de solução para o frasco. Não pipetar diretamente do frasco para evitar contaminações.
Informações espectrais:
| Técnica | Linhas (nm) | Limite de Detecção LD (mg/L) | Ordem | Tipo | Interferência |
|---|---|---|---|---|---|
| ICP-AES | 225,585 | 0,005 | 1 | íon | Fe, Ta, Ge, Ir, Cr |
| ICP-MS | 192 uma | 1 ppt | ----- | M+ | 176Yb16O, 176Lu16O, 176Hf16O, 192Pt |
| FAAS | 290,9 | 0,1 (N2O-acetileno) | 1 | átomo | A presença de peróxidos e/ou chama oxidante diminuem o sinal devido formação de OsO4 devido a queda de átomos livres. |