Tabela Periódica - Guia dos Elementos
Arsênio - As
Apresentação
Do Latim Arsenicum ou Grego Arsenikon identificado com Arsenikos, macho, pois se acreditava que os metais tinham sexo diferentes. Acredita-se que Albertus Magnus no século XIII obteve o elemento a partir do aquecimento do sulfeto de arsênio (ouropimenta) com sabão e Paracelso com casca de ovos. Apresenta-se em duas formas: amarelo ou cinza com brilho metálico. Forma-se compostos muito tóxicos. Quando aquecido forma óxido (As2O3) que se dissolve em bases formando os sais arsenitos. Se dissolve em ácido nítrico formando ácido arsênico (H3AsO4). É obtido atualmente como subproduto da mineração de prata e ouro.
Principais Características
O arsênio apresenta três estados alotrópicos: cinza ou metálico, amarelo e negro. O arsênio cinza metálico (forma α) é a forma mais estável nas condições normais e tem
estrutura romboédrica; é um bom condutor de calor, porém um péssimo condutor elétrico. O arsênio amarelo (forma γ) é obtido quando o vapor de arsênio é esfriado rapidamente.
É extremamente volátil e mais reativo que o arsênio metálico e apresenta fosforescência à temperatura ambiente. Também se denomina arsênio amarelo o mineral trissulfeto de
arsênio. Uma terceira forma alotrópica, o arsênio negro (forma ß), de estrutura hexagonal , tem propriedades intermediárias entre as formas alotrópicas descritas, e se
obtém da decomposição térmica da arsina ou resfriamento lento do vapor de arsênio. Todas as formas alotrópicas, exceto a cinza, não apresentam brilho metálico e apresentam
uma condutibilidade elétrica muito baixa, comportando-se como metal ou não-metal em função, basicamente, do seu estado de agregação.
Reage violentamente com o cloro e se combina, quando aquecido, com a maioria dos metais para formar o arsenieto correspondente; reage, também, com o enxofre. Não reage
com o ácido clorídrico em ausência de oxigênio, porém reage com o ácido nítrico aquecido, estando concentrado ou diluído, e com outros oxidantes como o peróxido de hidrogênio,
o ácido perclórico e outros. É insolúvel em água, porém muitos de seus compostos são solúveis. É um elemento químico essencial para a vida, ainda que tanto o arsênio como seus
compostos sejam extremamente venenosos.
Aplicações
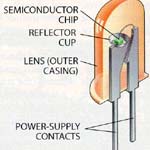
Conservante de couro e madeira (arseniato de cobre e crômio), uso que representa, segundo algumas estimativas, cerca de 70% do seu consumo mundial. O arsenieto de gálio é um importante semicondutor empregado em circuitos integrados mais rápidos e caros que os de silício. Aditivo em ligas metálicas de chumbo e latão. Inseticida (arseniato de chumbo), herbicidas (arsenito de sódio) e venenos. O dissulfeto de arsênio é usado como pigmento e em pirotécnica. Descolorante na fabricação do vidro (trióxido de arsênio). Recentemente renovou-se o interesse principalmente pelo uso do trióxido de arsênio para o tratamento de pacientes com leucemia.
História
O arsênio é conhecido desde tempos remotos assim como alguns de seus compostos, especialmente os sulfetos. Dioscórides e Plínio conheciam suas propriedades; Celso Aureliano, Galeno e Isidoro Largus sabiam de seus efeitos irritantes, tóxicos, corrosivos e sua ação parasiticida, e observaram suas virtudes contra a tosse, afecções da voz e dispnéia. Os médicos árabes usaram também compostos de arsênio em inalação, pílulas e poções, e também em aplicações externas. Durante a Idade Média os compostos arsenicais caíram no esquecimento sendo relegados aos curandeiros que os prescreviam contra algumas enfermidades. Roger Bacon e Alberto Magno se detiveram no seu estudo. O primeiro que o estudou em detalhes foi George Brandt en 1633, e Johann Schroeder o obteve em 1649 pela ação do carvão sobre o ácido arsênico. A Jöns Jacob Berzelius se devem as primeiras investigações acerca da composição dos compostos de arsênio. A partir do século XVIII os compostos arseniacais conseguiram um posto de primeira ordem na terapêutica até serem substituidos pelas sulfamidas e os antibióticos.