Molibdênio - Metodos de análises do molibdênio Mo
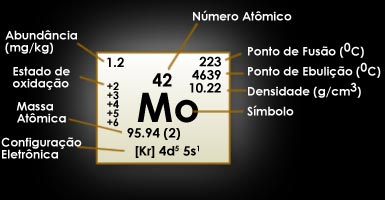
Descobrindo o elemento Molibdênio
|
Principais formas químicas em solução aquosa e coloração: Mo+6 como MoO42- (molibdato) (incolor)
Algumas propriedades químicas do elemento e reações: O molibdênio é um metal cinza com briho prateado, duro e que pertence ao grupo 6 e possui propriedades muito similares ao tungstênio. Em solução aquosa ocorre no estado de oxidação +6, principalmente na forma do ânion molibdato (MoO42-). Mas outros estados de oxidação podem ocorrer, variando de -4, -2 a +6, sendo o mais comum na forma sólida o Mo+4. O metal é bastante resistente a corrosão e não reage com a água. É muito resistente ao ataque de ácido como HCl, HNO3, H2SO4 diluídos a frio. Mas dissolve em ácido sulfúrico concentrado a quente. Facilmente solúvel em água régia formando MoO2Cl2 e também na mistura de HNO3:HF. Pouco atacado com soluções de bases. Quando aquecido com oxigênio quei- ma formando óxido. Reage em alta temperatura com carbono e nitrogênio formado carbeto e nitreto. Quando aquecido reage com os halogênios formando os respectivos haletos em diversos estados de oxidação. Aquecido com enxofre forma sulfeto (MoS2) com estrutura semelhante ao grafite e por isso usado em lubrificantes. Análise volumétrica: Alguns métodos volumétricos de análise de Mo são baseados na redução do Mo+6 para Mo+3 nas suas soluções. Como agentes redutores são empregados as amalgamas de zinco (redutor de Jones), tomando-se o cuidado de evitar contato com o oxigênio atmosférico. Após a redução do Mo, este pode ser titulado com permanganato de potássio. Também é usado para oxidar o Mo+3 formado, uma solução de sulfato férrico amoniacal que é adicionado em excesso e pode ser titulada com KMnO4. Também pode ser usado a solução de sufato de hidrazina para redução ao estado Mo+5 em meio HCl 1 ou 2M. Nessa condição o Mo+5 pode ser titulado usando solução de sulfato cérico e difenil bezidina como indicador. Análise Colorimétrica: O Mo pode ser determinado em soluções ácidos pela redução com SnCl2 e formação do complexo vermelho hexatiocianatomolibdato (III) [Mo(SCN)6]3- com excesso de tiocianato de sódio e em presença de H3PO4 (diferença do ferro). Esse complexo pode ser extraído com diversos solventes orgânicos como acetato de butila, éter ou álcool isoamílico. Para 15 mL de uma solução contendo 1 a 50 µg de Mo+6 adicionar 2 mL de ácido clorídrico 36%, 1 ml de solução de sal de Mohr a 1% em H2SO4 0,2N. Agitar e adicionar 3 mL de KCNS 10% (M/V) e 3 mL de SnCl2 a 10% em HCl 1,2M. Agitar. Diluir para 25 mL e adicionar exatamente 10 mL de álcool isoamílico para extrair o complexo de molibdênio. Agitar vigorosamente por 1 minuto e após decantar separar a fase or- gânica e ler as absorbâncias de padrões, branco e amostra em 475 nm. Sal de Mohr corresponde ao sal duplo (NH4)2SO4.FeSO4.6H2O. Análise por espectrometria e espectrofotometria atômica (principais linha analíticas) 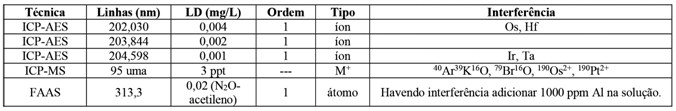
Espectro de emissão atômico do elemento de 400 a 700 nm Análise por fiuorescência de Raios X (XRF) em KeV (principais linhas espectrais) |